Спастичність – несприятливий фактор для відновлення пацієнтів з неврологічними захворюваннями

Вступ
Спастичність — це неврологічне порушення, яке проявляється підвищенням м’язового тонусу та може призводити до скутості м’язів, больового синдрому, зменшення об’єму рухів у суглобах, порушення рухових функцій і підвищення ризику падінь [1]. Окрім первинних рухових обмежень, спастичність асоціюється з розвитком вторинних ускладнень, зокрема контрактур і деформацій кінцівок, пролежнів, порушень сну, а також негативних змін психоемоційного стану, включно зі зниженням настрою та самооцінкою.
Спастичність є клінічним проявом багатьох неврологічних захворювань, зокрема мозкового інсульту, черепно-мозкової травми та нейродегенеративних процесів. З огляду на її поширеність і суттєвий негативний вплив на повсякденне функціонування пацієнтів, необхідність своєчасного й адекватного лікування спастичності є беззаперечною. Водночас значна частка пацієнтів не отримує належної терапії, що свідчить про недостатню увагу до цієї проблеми в широкій клінічній практиці.
Розробка ефективних і безпечних методів лікування спастичності, зокрема із застосуванням ботулінічного токсину, визначає актуальність і клінічну значущість даного питання [1]. Крім того, спастичність є одним із ключових чинників, що знижують ефективність реабілітаційних втручань у пацієнтів із тяжкими ураженнями нервової системи. Вона перешкоджає формуванню фізіологічних рухових патернів у процесі відновлення, тоді як своєчасна та цілеспрямована корекція спастичності може сприяти покращенню рухових функцій як у післягострому, так і в довготривалому періоді захворювання.
Визначення та класифікація спастичності
Зважаючи на те, що спастичність є не ізольованим феноменом, а одним із проявів ураження верхнього мотонейрона, а її патогенез досі залишається недостатньо вивченим, формулювання точного визначення спастичності є складним завданням. Перше визначення спастичності було запропоноване австралійським неврологом James W. Lance, який визначив її як «залежний від швидкості руху підвищений опір пасивним рухам кінцівки у осіб із синдромом ураження верхнього мотонейрона». Проте у визначенні Lance не враховується роль сенсорних порушень у розвитку спастичності.
У зв’язку з цим у 2005 році Програма з підтримки створення бази даних для оцінювання спастичності (Support Program for Assembly of a Database for Spasticity Measurement) запропонувала розширене розуміння спастичності, яке включає як нейрофізіологічні, так і клінічні аспекти цього стану. SPASM запропонувала оновлене визначення спастичності як «розладу сенсомоторного контролю, що виникає внаслідок ураження верхнього мотонейрона та проявляється періодичною чи стійкою мимовільною активацією м’язів». У цьому визначенні враховано як вплив в’язко-еластичних властивостей м’яких тканин на скутість кінцівок, що має особливе значення у осіб похилого віку, так і роль пропріоцепції та шкірних аферентних нервових шляхів.
Спеціально створена Міждисциплінарна робоча група з рухових розладів (Interdisciplinary Working Group for Movement Disorders) визначила спастичність у ширшому розумінні як «мимовільну гіперактивність м’язів за наявності центрального парезу». У цьому визначенні «мимовільна гіперактивність м’язів» розглядається як спектр клінічних проявів, що включає:
- спастичність у вузькому розумінні, яка провокується швидкими пасивними рухами в суглобах;
- ригідність, що виникає при повільних пасивних рухах у суглобах;
- дистонію, коли мимовільна гіперактивність м’язів виникає спонтанно;
- спазми — складні мимовільні рухи, які зазвичай спричинені сенсорними або звуковими подразниками.
Епідеміологія
Точні епідеміологічні дані щодо спастичності залишаються обмеженими. Вважається, що спастичність розвивається щонайменше у третини пацієнтів після інсульту [2]. За даними окремих досліджень, певний ступінь спастичності виникає у 38–40 % пацієнтів після інсульту, і близько 16 % з них потребують активного лікування. Zeng et al. повідомили, що частота спастичності залежить від часу оцінювання і варіює від 27 % через один місяць після інсульту до 42,6 % у віддаленому періоді (понад 3 місяці від початку захворювання) [3,4]. Інші автори також зазначають зростання поширеності спастичності з часом — від 19 % через 3 місяці після мозкового інсульту до 21,7 % та 42,6 % через 4 і 6 місяців відповідно [5].
Хоча у більшості пацієнтів спастичність формується протягом перших трьох місяців від початку захворювання, в окремих випадках вона може розвиватися пізніше, що зумовлює необхідність оцінювання спастичності як у післягострому, так і у довготривалому періоді.
Результати досліджень свідчать, що спастичність спостерігається у 34–84 % пацієнтів після черепно-мозкової травми середнього та тяжкого ступеня. Поширеність спастичності при ураженні спинного мозку коливається від 40 % до 78 %. За даними Holtz et al. (2016), частота спастичності після спінальної травми сягає 65 %, при цьому близько 35 % пацієнтів мають спастичність, яка важко піддається лікуванню [6].
Церебральний параліч діагностується приблизно у 1,5–4,0 на 1000 новонароджених і є найпоширенішою причиною інвалідності серед дітей. При цьому спастичність становить провідний компонент рухових порушень майже у 80 % пацієнтів. Приблизно 67 % пацієнтів із розсіяним склерозом мають ті чи інші прояви спастичності, з них 38 % — помірну або тяжку спастичність, що призводить до обмеження повсякденної життєдіяльності [7].
Наявність спастичності зумовлює численні негативні наслідки, які призводять до значних функціональних обмежень та зниження якості життя пацієнтів. Крім того, спастичність є суттєвим економічним тягарем для будь-якої країни, оскільки значно обмежує працездатність дорослого населення та часто потребує залучення стороннього догляду.
Патофізіологія спастичності
Патофізіологія розладів м’язового тонусу на сьогодні залишається предметом інтенсивного вивчення у зв’язку з багатокомпонентним впливом різних структур головного і спинного мозку на стан та функції сенсомоторного апарату. Ключовою ланкою патогенезу спастичності є порушення центральної регуляції м’язового тонусу, яка забезпечується складною взаємодією гальмівних та активуючих впливів різних відділів центральної нервової системи. Спастичність виникає внаслідок порушення взаємодії спінальних і супраспінальних нейротрансмітерних систем із подальшими компенсаторними змінами в усіх структурах, що регулюють мимовільні та довільні рухові акти. Спінальний компонент спастичності може бути зумовлений як підвищенням збуджувальної активності, так і зменшенням гальмівного впливу. До основних патофізіологічних причин розвитку спастичності належать: гіперзбудливість спінальних інтернейронів, підвищення збудливості рецепторів, формування нових синапсів унаслідок аксонального спраутингу, посилення взаємодії гамма-мотонейронів з інтрафузальними м’язовими волокнами, а також підвищена збудливість альфа-мотонейронів [8].
Експериментальні тваринні моделі продемонстрували важливу роль мембранних властивостей мотонейронів у формуванні спастичності. Залежний від напруги постійний іонний струм, опосередкований натрій- та кальційзалежними каналами, може спричиняти тривалу деполяризацію мотонейронів, яка модулюється низхідною серотонінергічною та норадренергічною регуляцією. У гострій фазі спінальної травми через втрату низхідного моноамінергічного впливу у вентральних рогах спинного мозку виникає гіпоактивація рухових нейронів, тоді як у дорсальних рогах — дезінгібіція та підвищення збудливості сенсорного входу. Водночас, попри міжнейронну гіперзбудливість, спастичність не розвивається негайно, а формується лише після відновлення збудливості мотонейронів. У хронічній фазі у мотонейронах вентральних рогів виникає денерваційна гіперчутливість до залишкового моноамінергічного впливу, активується постійний іонний струм, що сприяє розвитку спастичності. Окрім збуджувальних механізмів, що сприяють формуванню спастичності, дедалі більше уваги в сучасних дослідженнях приділяється ролі змінених спінальних інгібіторних схем [9].
При ураженнях спинного мозку можливі декілька патофізіологічних варіантів:
- Неповна (часткова) мієлопатія з ураженням бічного канатика. Якщо залучений лише кортикоспінальний тракт, виникають слабкість, гіпотонія та втрата поверхневих рефлексів. При додатковому ураженні дорсального ретикулоспінального тракту розвиваються спастичність і гіперрефлексія через необмежену активність медіального ретикулоспінального тракту. У цьому випадку спастичність переважає в антигравітаційних м’язах. Якщо ж уражений ретикулоспінальний тракт, а кортикоспінальний залишається інтактним, можлива спастичність без значної м’язової слабкості.
- Повна мієлопатія з ураженням усіх чотирьох низхідних шляхів. У цьому випадку спастичність може бути менш вираженою через відсутність активуючого впливу з боку медіального ретикулоспінального та медіального вестибулоспінального трактів. Пригнічення аферентного згинального рефлексу призводить до розвитку парезу з підвищенням тонусу згиначів [10].
З плином часу до нейрогенного компонента спастичності приєднується біомеханічний: зниження еластичності та вкорочення м’язів, структурні зміни сухожилків і навколишніх тканин, що істотно погіршує клінічну картину. За відсутності адекватної корекції спастичності поступово формується безперешкодне тривале скорочення уражених м’язових груп (спастична дистонія), яке призводить до патологічної установки кінцівки. Це, у свою чергу, перешкоджає подовженню м’язів і посилює прояви спастичності. Натомість ранній початок лікування дозволяє покращити функціональні результати реабілітації [1].
Вплив спастичності на життя пацієнта та його родини
Спастичність суттєво впливає на функціональний стан пацієнтів із тяжкими неврологічними захворюваннями та є однією з ключових причин обмеження відновлення. Вона порушує якість рухів, знижує мобільність і здатність до самообслуговування, негативно впливає на сон, психоемоційний стан і соціальну активність пацієнта, що безпосередньо відображається на якості життя.
У післягострому періоді відновлення незначне або помірне підвищення м’язового тонусу, зокрема у розгиначах нижніх кінцівок, у деяких пацієнтів може тимчасово сприяти стабілізації положення тіла та підтримці функції ходи. Однак за відсутності своєчасної корекції прогресування спастичності призводить до формування контрактур, деформацій суглобів і стійких патологічних рухових установок. На цьому етапі рухові обмеження поєднуються з труднощами у виконанні повсякденних дій, зростає залежність пацієнта від сторонньої допомоги, що істотно погіршує його функціональну незалежність.
Біль є частим і клінічно значущим супутнім проявом спастичності. У більшості пацієнтів він має змішаний характер і поєднує нейропатичний та ноцицептивний компоненти. Ноцицептивний біль виникає внаслідок хронічного перенавантаження м’язів і сухожилків, тоді як тривале патологічне скорочення м’язів з часом призводить до структурних змін м’язової тканини, включно з фіброзом і атрофією. Наявність больового синдрому незалежно від ступеня підвищення м’язового тонусу свідчить про необхідність раннього та комплексного підходу до лікування спастичності.
Принципи втручання у фізичній терапії
На сьогодні відсутні докази існування фізіотерапевтичного втручання з довготривалим ефектом, спрямованого виключно на зменшення спастичності. Більшість досліджень демонструють лише короткочасний ефект (динамічні шини з лайкри, вібрація м’язів-антагоністів тощо) [11].
Фізичний терапевт повинен враховувати, що після введення ботулотоксину зменшується рівень спастичності, але СВМК не змінюється. Тому втручання мають бути спрямовані на:
- навчання контролю м’язової активності;
- виконання функціональних завдань;
- підтримку еластичності м’яких тканин;
- використання ортезів для біомеханічної корекції.
Пасивний розтяг
Пасивний розтяг тривалий час вважався базовим втручанням при спастичності, проте сучасні клінічні настанови не рекомендують його як основний метод лікування у пацієнтів після інсульту. Клінічна значущість мінімального збільшення пасивної амплітуди рухів залишається сумнівною. Тому пасивний розтяг не слід використовувати як провідне втручання.
Силові тренування та контроль м’язової активності
Сучасні дослідження показали, що силове тренування не підвищує рівень спастичності, а спастичні м’язи часто є слабкими. Особливо ефективними є вправи з ексцентричним скороченням, які сприяють формуванню контролю м’язової активності та можуть бути оптимізовані за допомогою ортезування [12]. До реабілітаційної програми пацієнта доцільно включати IVS-терапію.
Оцінка пацієнта та постановка цілей
Оцінка включає:
- детальне опитування;
- фізикальне обстеження;
- оцінку СВМК, сили, тонусу, чутливості;
- аналіз когнітивних та мовних порушень.
Для оцінки спастичності рекомендовано використання модифікованої шкали Ешворта (mAS). Також у пацієнтів з наслідками ЧМТ та ДЦП можна використовувати шкалу дистонії Баррі Олбрайта (Barry Albright Dystonia Scale, BADS). Для оцінки діяльності та участі — функціональні тести (Leeds Adult Spasticity Impact Scale, 10-метровий тест ходи тощо).
Постановка цілей
Постановка реабілітаційних цілей при спастичності має здійснюватися в межах мультидисциплінарного підходу із залученням лікаря фізичної та реабілітаційної медицини, фізичного терапевта, ерготерапевта та, за потреби, інших фахівців. Визначення цілей повинно ґрунтуватися не лише на клінічних показниках, а й на функціональних потребах пацієнта та умовах його повсякденного життя. Активна участь пацієнта в обговоренні стратегії реабілітаційної допомоги є обов’язковою, оскільки сприяє формуванню реалістичних цілей, підвищує мотивацію та покращує комплаєнс і функціональні результати лікування. Рекомендовано використовувати формат SMART: конкретна, вимірювана, досяжна, доречна, обмежена в часі.
Сучасні методи лікування: ботулінотерапія та кріотерапія
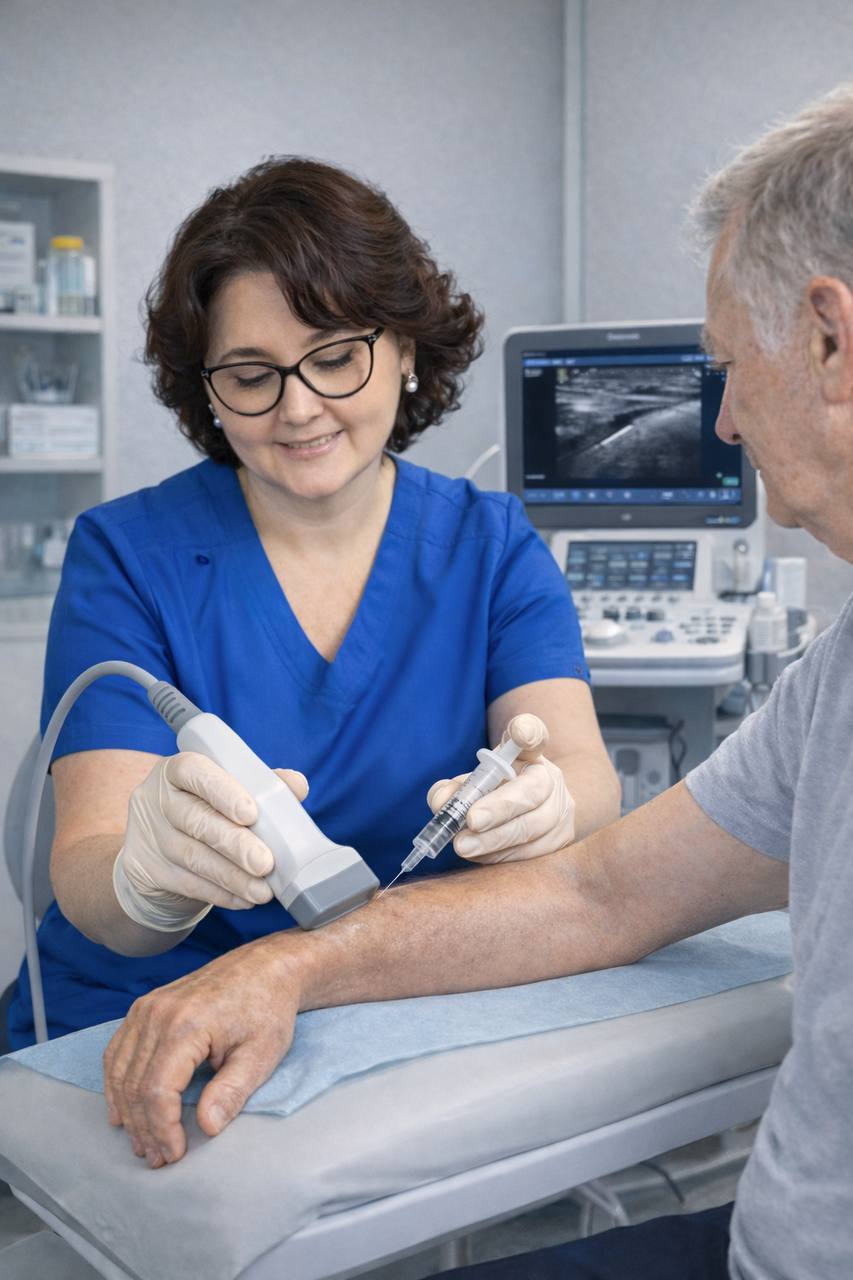
Золотим стандартом лікування фокальної та сегментарної спастичності є введення ботулінічного нейротоксину типу A під ультразвуковим контролем. Використання ультразвукової навігації забезпечує точну візуалізацію цільових м’язів, зменшує ризик ураження суміжних анатомічних структур та підвищує ефективність і безпеку ін’єкцій.
З метою знеболення під час введення ботулінічного нейротоксину може застосовуватися локальна кріотерапія, яка дозволяє знизити інтенсивність больових відчуттів без впливу на фармакодинаміку препарату та без використання системних аналгетиків. Використання кріотерапії є доцільним як у дорослих, так і у дітей, особливо за необхідності багаторазових ін’єкцій.

В нашому відділенні ми успішно використовуємо інноваційний прилад локальної кріотерапії Cryo 7 від німецького виробника Zimmer MedizinSysteme, створений для безпечного та результативного охолодження тканин з метою зниження запалення, знеболення та прискорення відновлення. Ефект зниження запалення та болю зберігається протягом 90–180 хвилин, залежно від стану пацієнта та тривалості процедури (від 30 секунд до 10 хвилин).
На відміну від інших методів охолодження, таких як контактне охолодження, кріоспреї або льодові пакети, Cryo 7 швидше знижує температуру шкірних покривів з меншим ризиком отримати холодовий опік, а також підтримує постійну температуру охолодження протягом усієї процедури. Такий підхід робить введення препарату безболісним та безпечним.
Висновки
Спастичність є одним із ключових чинників, що обмежують функціональне відновлення та формування незалежності у пацієнтів. Вона має багатовимірний вплив на рухову функцію, біль, здатність до самообслуговування та якість життя, а при відсутності своєчасної корекції призводить до розвитку вторинних структурних змін, контрактур і стійкої інвалідизації.
Ефективне лікування спастичності потребує комплексного, індивідуалізованого підходу з урахуванням нейрофізіологічних і біомеханічних механізмів її розвитку. Застосування ботулінічного нейротоксину типу A під ультразвуковим контролем залишається золотим стандартом лікування фокальної та сегментарної спастичності, забезпечуючи безпечне та цілеспрямоване зниження м’язової гіперактивності. Використання локальної кріотерапії як методу знеболення під час ін’єкцій підвищує комфорт пацієнтів і покращує переносимість лікування.
Фармакологічна корекція спастичності створює терапевтичне «вікно можливостей» для реалізації реабілітаційних втручань, однак не може розглядатися як самостійний метод відновлення. Поєднання медикаментозного лікування з індивідуалізованою програмою фізичної терапії та сучасними нейрореабілітаційними технологіями, зокрема IVS-терапією, дозволяє впливати на центральні механізми спастичності, покращувати контроль рухів і підвищувати ефективність відновлення.
Використання об’єктивних інструментів оцінки та можливість моніторингу динаміки пацієнта в процесі лікування є важливою складовою сучасного менеджменту спастичності. Такий підхід дозволяє своєчасно коригувати реабілітаційну стратегію, оптимізувати функціональні результати та сприяти покращенню якості життя пацієнтів.
Список літератури
- О. С. Цуркаленко, М. Я. Романишин, О. Л. Кушнеренко, І. Р. Гаврилів, Ю. В. Фломін, М. В. Гуляєва, Л. В. Федоришин, С. В. Фєдосєєв, М. С. Бровченко, В.Ф. Рассохін, К.О. Карпінська, Є.І. Цьома, О.О. Левківський, Л.Є. Осадча. Лікування спастичності з використанням ботулінічного нейротоксину типу А: Наукове положення Української асоціації боротьби з інсультом та Української асоціації фізичної терапії. – 2021 – №2 – С. 4-23.
- Graham LA. Management of spasticity revisited. Age Ageing. 2013; 42 (4): 435.
- Wissel J, Fheodoroff K, Hoonhorst M, Müngersdorf M, Gallien P, Meier N, Hamacher J, Hefter H, Maisonobe P, Koch M. Effectiveness of AbobotulinumtoxinA in Post.
- Zeng H, Chen J, Guo Y, Tan S. Prevalence and Risk Factors for Spasticity After Stroke: A Systematic Review and Meta.
- Auttidren with cerebral palsy: an overview of review articles. Am J Phys Med Rehabil. 2006; 85 (1): 89.
- Holtz KA, Lipson R, Noonan VK, Kwon BK, Mills PB. Prevalence and Effect of Problematic Spasticity After Traumatic Spinal Cord Injury. Arch Phys Med Rehabil. 2017; 98 (6): 1132.
- McGuire J. Epidemiology of spasticity in the adult and child. In: Brashear A, Elovic E, editors. Spasticity, diagnosis and treatment. 1st edition. Demos<15.
- Ditunno JF, Little JW, Tessler A, Burns AS. Spinal shock revisited: a four phase model. Spinal Cord. 2004; 42 (7): 383-95.
- Crone C, Petersen NT, Gimenéz Roldán S, Lungholt B, Nyborg K, Nielsen JB. Reduced reciprocal inhibition is seen only in spastic limbs in patients with neurolathyrism. Exp Brain Res. 2007; 181 (1): 193-7.
- Ganguly J, Kulshreshtha D, Almotiri M, Jog M. Muscle Tone Physiology and Abnormalities. Toxins (Basel). 2021; 13 (4): 282.
- Gracies JM et al. Safety and efficacy of abobotulinumtoxinA for hemiparesis in adults with upper limb spasticity after stroke or traumatic brain injury: a double-blind, randomized, placebo-controlled trial. Lancet Neurol. 2015.
- Morris C. A review of the efficacy of lower-limb orthoses used for cerebral palsy. Dev Med Child Neurol. 2002; 44 (3): 205-11.
Сучасний стандарт знеболення: система локальної кріотерапії Cryo 7
Автор допису

Маріанна Бровченко
Завідувач відділення фізичної та реабілітаційної медицини КНП «Київська міська клінічна лікарня № 18», кандидат медичних наук, доцент кафедри реабілітаційної медицини, фізичної терапії та спортивної медицини Національного університету охорони здоров’я України імені П. Л. Шупика.
